
화학실험을 하면 많이 쓰는 단위 중의 하나는 몰수이다. 왜냐면 몰수만 알면 물질의 질량이나 수를 계산할 수 있기 때문에 나름 편리하다. 역으로 질량이나 수를 안다면 몰수를 계산할 수 있다. 계산하는 방법에 대하여 알아보자.
| 몰수로 질량 계산하기 |
몰(mol)의 단위를 질량의 단위(g)로 바꾸기 위해서는 몰 질량이라는 환산 인자로 사용하면 된다. 몰 질량이랑 1몰당 질량이 얼마나 있는지를 말하며 단위는 (g/mol)이다. 식을 써보자면

예를 들어 질소(N₂)는 몰 질량이 28g/mol이다. 3mol의 질소의 질량을 구하면 3 x 28 = 84g이 된다.
| 질량으로 몰수 계산하기 |
역으로 질량을 알 경우 몰수를 구할 수도 있다. 질량에다가 몰질량을 나누면 된다.
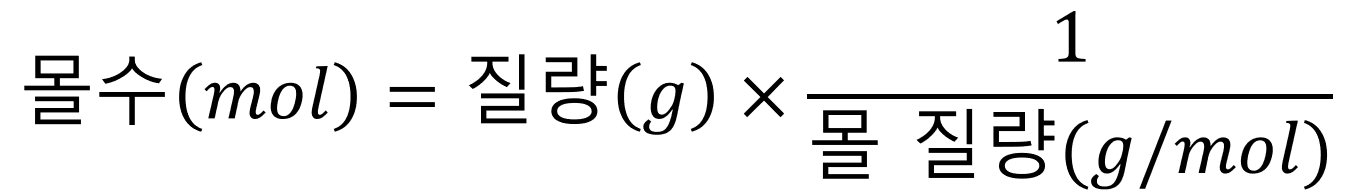
140g의 질소의 질량을 구하기 위해 몰질량을 나눠보자. 140/28 = 5mol이 된다.
| 원자 혹은 분자의 개수 계산하기 |
아보가드로의 법칙에 의하면 1mol당 분자 혹은 원자의 개체수는 6.022 x 10²³개다. 이것을 아보가드로 수라고 한다 여하튼 간에 엄청 많다. 이것인 우리가 몰수를 개체수를 알아보고자 할 때 쓸 수 있는 환산 인자다. 몰수를 알면 개체수를 알 수 있고, 몰수는 앞서 말했듯이 물질의 질량을 알면 구할 수 있다.
정리하면 물질의 몰수, 혹은 질량을 안다면 개체수를 구할 수 있다는 것이다. 구하는 것은 간단하다.
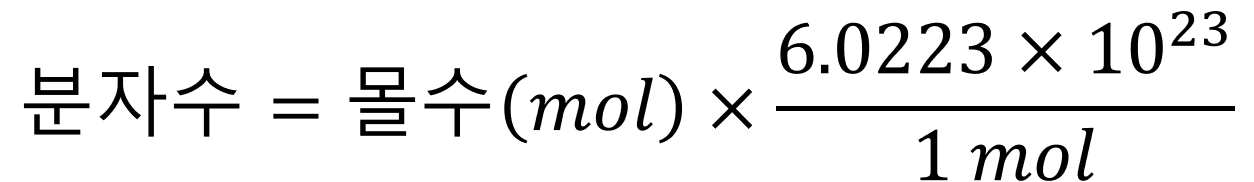
최종적으로 앞서 언급하였던 예로 개체수를 구해보자
140g의 질소의 개체수를 구해보자.
140/28 = 5mol ← 몰질량(28g/mol)을 통한 몰수 계산
5mol x [6.022 x 10²³/mol] = 30.022 x 10²³개 ← 아보가드로수를 통한 개체수 계산
'과학 > 화학' 카테고리의 다른 글
| 보일의 법칙에 대하여 알아보자 (0) | 2021.10.25 |
|---|---|
| [화학] 화합물의 질량 분율 구하기 (0) | 2020.10.05 |
| 기체상수 R을 다양하게 단위변환 하기 (0) | 2019.05.14 |
| 기체상수 R 구하기 (3) | 2019.05.09 |
| [기체의 상태방정식]이상기체 상태방정식 (1) | 2019.04.29 |