화학이든 열역학이든 공부하다 보면 이상기체 방정식은 질리도록 볼 것이다.
그리고 항상 기체상수 R이라는 것이 따라올 것이다. 수치는 정해져 있다. 이 수치는 왜 나온 걸까?
이상기체 상태 방정식 PV=nRT에서 R값이 어떻게 구해지는지를 알아보자.
이상기체 방정식에서 V는 아보가드로의 법칙에 의해 등온, 등압에서 항상 일정한 값을 가진다.
아보가드로 법칙이란 같은 온도와 압력 하에서 모든 기체는 같은 부피 속에 같은 수의 분자가 있다는 것을 말한다.
그래서 과학자들은 이상기체가 T : 0℃, P : 1 atm의 조건에서 부피는 22.4ℓ가 된다라고 정확한 수치로 표현했다.
여기서 기체의 몰수를 1㏖로 정의하고 이상기체 방정식을 R로 정리해보자.

여기에서 T : 0℃, P : 1 atm, V : 22.4ℓ 를 대입해보자. 그전에 T=0℃는 절대온도 단위로 고쳐서 T = 273K를 대입하자.
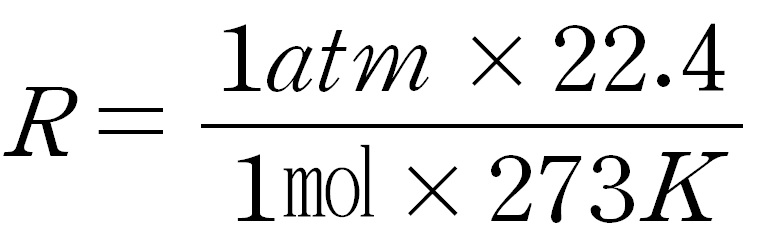

물론 이 값도 많이 쓰이기는 한다. 하지만 보통 8.314J/㏖*K가 많이 친숙할 것이다. 이걸로 한번 바꿔보자.
바꾸려면 어떻게 해야 할까? atm*L을 J로 바꿔야 한다. 바꿔보자.

자 그럼 이제 atm*L을 J로 바꿔주면 된다. 바꿔보자

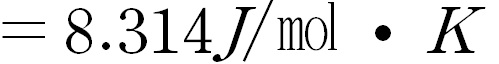
이렇게 하면 우리에게 친숙한 R값을 구할 수 있다.
가끔 단위 변환하는데 헷갈려하는 사람들이 많기에 독자들의 참고용으로 필자가 보통 단위 변환할 때 쓰는 계산방식으로 계산을 해보았다. 저렇게 분수로 적은 뒤 소거되는 단위를 하나하나 없애나 가는 방식이 속도를 떠나서 실수가 가장 적었다. 사람마다 물론 방식이 다르겠지만 난 저 방법을 적극 추천한다.
'과학 > 화학' 카테고리의 다른 글
| 보일의 법칙에 대하여 알아보자 (0) | 2021.10.25 |
|---|---|
| [화학] 화합물의 질량 분율 구하기 (0) | 2020.10.05 |
| [화학] 물질의 몰, 질량 및 분자 수 계산하기 (0) | 2020.09.27 |
| 기체상수 R을 다양하게 단위변환 하기 (0) | 2019.05.14 |
| [기체의 상태방정식]이상기체 상태방정식 (1) | 2019.04.29 |